首款国产新冠药停产,4.4亿元研发投入换来5160万元营收!
- 2023-03-28 18:00:22 健康一线
- 健康
商业化8个月后,首款国产新冠中和抗体疗法官宣停产。
3月24日,腾盛博药发布公告称,决定停止生产旗下控股子公司腾盛华创医药技术(北京)有限公司(下称“腾盛华创”)研发的新冠病毒中和抗体联合治疗药物安巴韦单抗注射液(amubarvimab,BRII-196)及罗米司韦单抗注射液(romlusevimab,BRII-198)。
公告进一步指出,这一决定是基于不断演变的新冠疫情趋势和相关政策的更新,包括美国卫生与公众服务部(HHS)计划于2023年5月结束新冠疫情国家紧急状态和公共卫生紧急状态(PHE),以及医药合同定制研发生产企业(CDMO)对药物相关情况的长时间观察。
财报显示,2022年,腾盛博药营收由零增加至5160万元,均来自安巴韦单抗╱罗米司韦单抗联合疗法。其研发开支为4.41亿元,行政开支为人民币1.69亿元,销售及营销开支为2686万元,年内亏损约4.84亿元。
对于此次停产后,是否还有剩余库存,腾盛博药相关负责人回应《华夏时报》记者称:“我们已基本将该药物的全部适销产品销售到全国25个省份了。”
01
去年销售额5160万元
2021年12月8日,作为国产首个新冠中和抗体疗法,腾盛博药的安巴韦单抗和罗米司韦单抗联合疗法获批在国内上市,用于治疗轻型和普通型且伴有进展为重型(包括住院或死亡)高风险因素的成人和青少年(12—17岁,体重≥40 kg)新型冠状病毒感染(COVID-19)患者,其中青少年适应症人群为附条件批准。
据此前甘肃省公共资源交易中心挂网信息,安巴韦单抗和罗米司韦单抗联合疗法挂网单价为“每支不高于全国最低价2417元”,由此推算,每人治疗费用近万元。
腾盛博药表示,2022年7月在中国商业化上市后,公司已基本将安巴韦单抗╱罗米司韦单抗联合疗法的全部适销产品出售给全国25个省份及358家医院,该药在2022年实现销售收入约5160万元。作为确保人道主义通道及为遏制疫情暴发作出贡献的承诺的一部分,腾盛博药于商业化上市前向中国21个城市及22家医院捐赠近3000人份的该抗体用于紧急使用。
3月24日,腾盛博药公告称,公司已作出决定结束安巴韦单抗╱罗米司韦单抗联合疗法项目,并已停止生产工作以将资源重新转向核心项目。同时,公司预计,未来无论在中国或美国以及其他地区,都不会再从该联合疗法中产生可观收入。
财报显示,2022年,公司营收由零增加至5160万元,均来自安巴韦单抗╱罗米司韦单抗联合疗法。其研发开支为4.41亿元,行政开支为人民币1.69亿元,销售及营销开支为2686万元,年内亏损约4.84亿元。2022年底流动资产为30.77亿元,其中现金及现金等价物11.9亿元。
记者查询发现,腾盛博药拥有一条针对传染病及CNS疾病的由10多个创新候选产品组成的管线,核心候选药物为治疗乙型肝炎病毒、人类免疫缺陷病毒HIV等传染病的药物,但除安巴韦单抗╱罗米司韦单抗联合疗法外,其余均处于临床早期阶段,进入临床2期的只有4项。
进展最快的是由VBI及Vir授权的乙型肝炎项目,目前正在开展BRII-179(一种新型重组蛋白免疫疗法)和BRII-835 (一种经皮下注射给药的靶向HBV病毒RNA的siRNA药物)联合治疗乙肝的研究。财报称,2022年2月,2期MRCT联合疗法研究已完成90名亚太地区患者入组。
对于研发进展,腾盛博药坦言,“由于我们的大多数候选药物仍在进行临床试验以及COVID-19项目被终止,我们预计未来很短期内不会实现候选药物销售或商业化。2022年,我们重新关注作为该领域行业领跑者的中国HBV的核心开发项目,以及精神障碍治疗项目,目前正在美国加速精神障碍治疗相关的临床开发。”
02
停产并非个例
对于新冠中和抗体的停产,市场似乎并不感到意外。
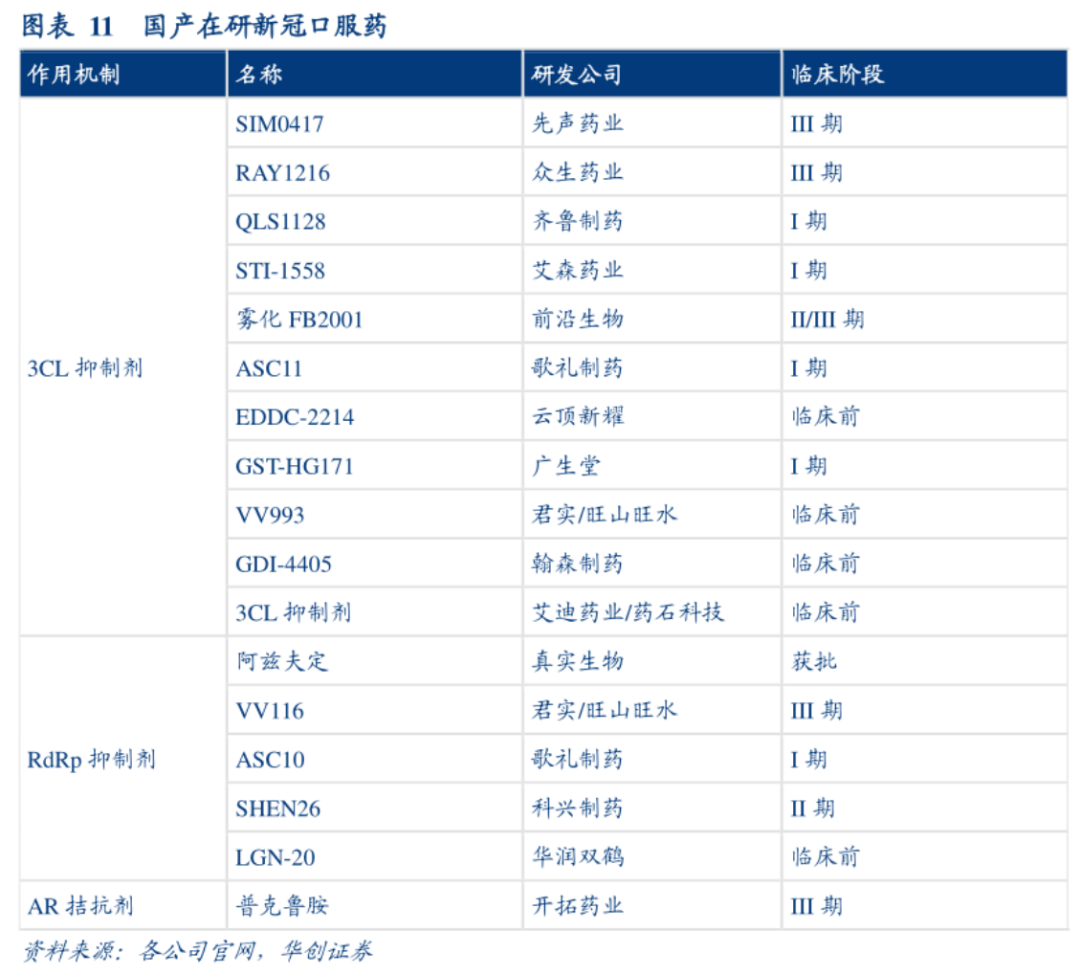
中和抗体是指由B淋巴细胞产生的,能识别抗原特异性部位而使抗原失去活性,抑制其功能的抗体,也被称为保护性抗体。据不完全统计,目前,全球已有20款中和抗体药物获批临床,国内在研治疗新冠中和抗体药物至少有10款。
整体来看,全球已有6款中和抗体或组合疗法获得紧急使用授权,包括此前获批的再生元casirivimab/imdevimab联合疗法、礼来/君实生物合作开发的etesevimab/bamlanivimab联合疗法、葛兰素史克与Vir Biotechnology合作研发的Sotrovimab。
尽管赛道火热,但中和抗体的疗效,一直被业内质疑。
病毒学专家常荣山此前接受本报记者采访时表示,新冠病毒流行株的迭代很快,平均6个月左右。抵抗不同的变异株,需要的中和抗体(抗体特异性)是不同的,半数抑制浓度也是不同的,这两个指标能说明抗体药物的有效性,此外,维持保护时长也是一个重要指标,因此中和抗体的保护力值得关注。
事实确实如此,随着病毒不断变异,中和抗体一度因为疗效不足出现被停止使用的情况。
2022年3月28日,根据美国食品和药物管理局(FDA)的最新指示,全美有8个州将停止使用葛兰素史克和Vir Biotechnology联合研发的新冠抗体疗法。FDA声明称:“对具有高度传播性的奥密克戎BA.2变体而言,于2021年5月获得紧急使用授权(EUA)的葛兰素史克新冠抗体疗法sotrovimab可能不太有效,不适用于大规模流行的的BA.2病毒株。”
更早一些的2022年1月24日,FDA宣布限制再生元、礼来/君实新冠中和抗体的使用,因这两款抗体对Omicron突变株无效,除非患者感染的是对这些新冠中和抗体敏感的突变株如Delta,医生才可以对患者使用这两款抗体。据再生元2022年财报,自限制使用以来,REGEN-COV在美国的销售业绩瞬间降至冰点,为0销售。
或许同样是基于疗效不佳的原因,2023年1月下旬,FDA撤销了对阿斯利康Evusheld的EUA,自此,在美国投入使用的六款中和抗体全线败退。而正在排队申请EUA的中和抗体,也成为了明日黄花。
2022年4月,再生元宣布FDA延长了REGEN-COV用于治疗和预防新冠肺炎的上市申请审查,PDUFA日期是2022年7月13日,但至今仍未有更多消息披露。
2021年10月,腾盛博药就宣布其在研的中和抗体联合疗法已经向美国FDA提交了紧急使用授权(EUA)申请。如今,两年过去,等来的却是停产和撤回的消息。
“公司正在与美国FDA沟通,在完成所有监管要求后,适当的时候撤回EUA申请,并会与中国国家药品监督管理局(NMPA)进一步沟通,在2023年第三季度完成监管机构的各项要求后,撤回生物制品许可申请(BLA)。”腾盛博药相关负责人向《华夏时报》记者透露。
至于其他一度被热议的中和抗体资产,诸如迈威生物9MW3311 、神州细胞SCTA01、绿叶制药LY-CovMab、复宏汉霖HLX70、济民可信JMB2002等等名字,恐怕已经成为掘金路上的一个分母。
与此同时,还有一系列在研国产小分子新冠药物的命运也成疑...
来源:华夏时报

本文地址://www.styjt.com/jiankang/2023-03-28/633852.html
友情提示:文章内容为作者个人观点,不代表本站立场且不构成任何建议,本站拥有对此声明的最终解释权。如果读者发现稿件侵权、失实、错误等问题,可联系我们处理
- 终结结核流行路在何方?专家:还需革新策略和技术2023-03-28 18:00:34
- 国外应对青少年心理健康问题的支持服务2023-03-28 18:00:33
- 日本专家:坚决反对核污水排海2023-03-28 18:00:33
- 韩国有意解禁福岛水产品?在野党呼吁韩总统表态2023-03-28 18:00:32
- 美国加州海獭死于罕见寄生虫菌株 研究人员称或也威胁人类2023-03-28 18:00:32

 70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗
70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗2022-11-07

 梅婷现任70岁老公曾剑个人资料(曾剑个人资料)
梅婷现任70岁老公曾剑个人资料(曾剑个人资料)2022-09-08
- 烟台今天已封闭的小区 烟台现在封闭小区名单有哪些
2022-10-12 09:07:30
- 张家界桑植新娘吴梅婚纱照事件完整版 看女主出轨聊天内容视频
2022-11-11 14:27:00
- 无人售货机功能(无人自动售货机操作方法介绍)
2022-07-27 08:41:09
- 目前南岸区及江北封闭小区名单有哪些 看最新封控通告
2022-11-11 14:49:26
- 2022南宁封控小区名单表 南宁最新封闭小区名单2022年8月什么情况
2022-08-26 09:52:30
文章排行榜
- 周排名
- 月排名