Advanced Materials:洪佳旭/何耀团队在眼科细菌感染性疾病中首次实现ASO向人类耐药菌的特异性递送
- 2023-04-26 18:00:18 健康一线
- 健康
在临床治疗中,为了节省宝贵的时间,医生通常在获得准确诊断之前给患者开具广谱抗生素。然而,抗生素的过度使用往往会促进抗生素耐药(ABR)细菌的出现。此外,广谱抗生素不仅能杀灭致病菌,还会杀灭有益菌。
近年来,CRISPR-Cas疗法、工程毒素、抗菌肽开始被用作抗菌药物,与这些抗菌剂不同的是,反义寡核苷酸(ASO)可以靶向特定的细菌基因并通过碱基互补配对的方式抑制其转录,从而显著扩大了可用的治疗靶点,在抗生素耐药(ABR)细菌中也同样如此。
但需要注意的是,ASO与其互补基因结合并发挥抑制作用的前提是将其有效递送到细菌细胞内。然而,由于独特的细菌质膜和细胞壁施加的静电电荷或尺寸屏障,常规ASO很难自由进入细菌细胞中。而目前用于递送的ASO的载体无法区分细菌细胞和哺乳动物细胞。这极大地阻碍了细菌感染的临床前或临床治疗,特别是那些由抗生素耐药细菌引起的感染。
近日,复旦大学附属眼耳鼻喉科医院洪佳旭主任医师、苏州大学何耀教授、王后禹研究员等在 Advanced Meterials 期刊发表了题为:Antisense Oligonucleotides Selectively Enter Human-derived Antibiotic-Resistant Bacteria through bacterial-specific ATP-binding Cassette Sugar Transporter 的研究论文。
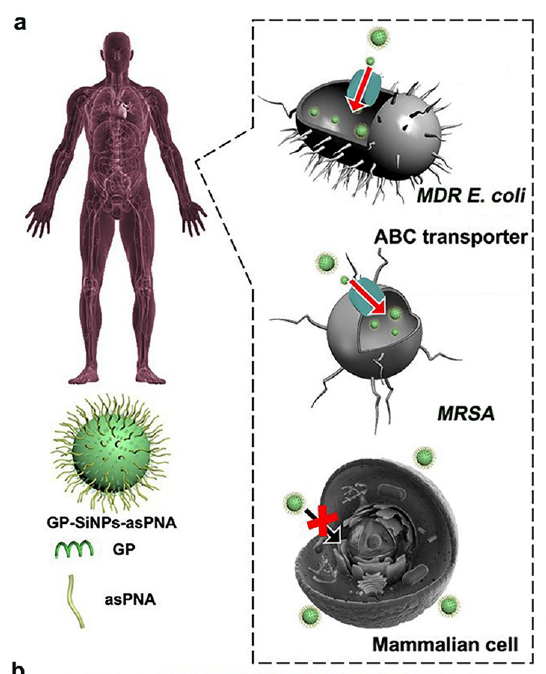
该研究利用了细菌特异性ATP结合盒(ABC)糖转运体,通过将ASO搭便车到α(1-4)-糖苷连接的葡萄糖聚合物(GP)上,从而让细菌选择性摄取并内化ASO。
与非特异性被哺乳动物和细菌吞噬的细胞穿膜肽相比,由葡萄糖聚合物和反义多核酸修饰的纳米颗粒组成的治疗药物(GP-SiNPs-asPNA)被选择性地内化到人类来源的多重耐药大肠杆菌和耐甲氧西林金黄色葡萄球菌中,并且显示出更高的摄取率(51.6%)。
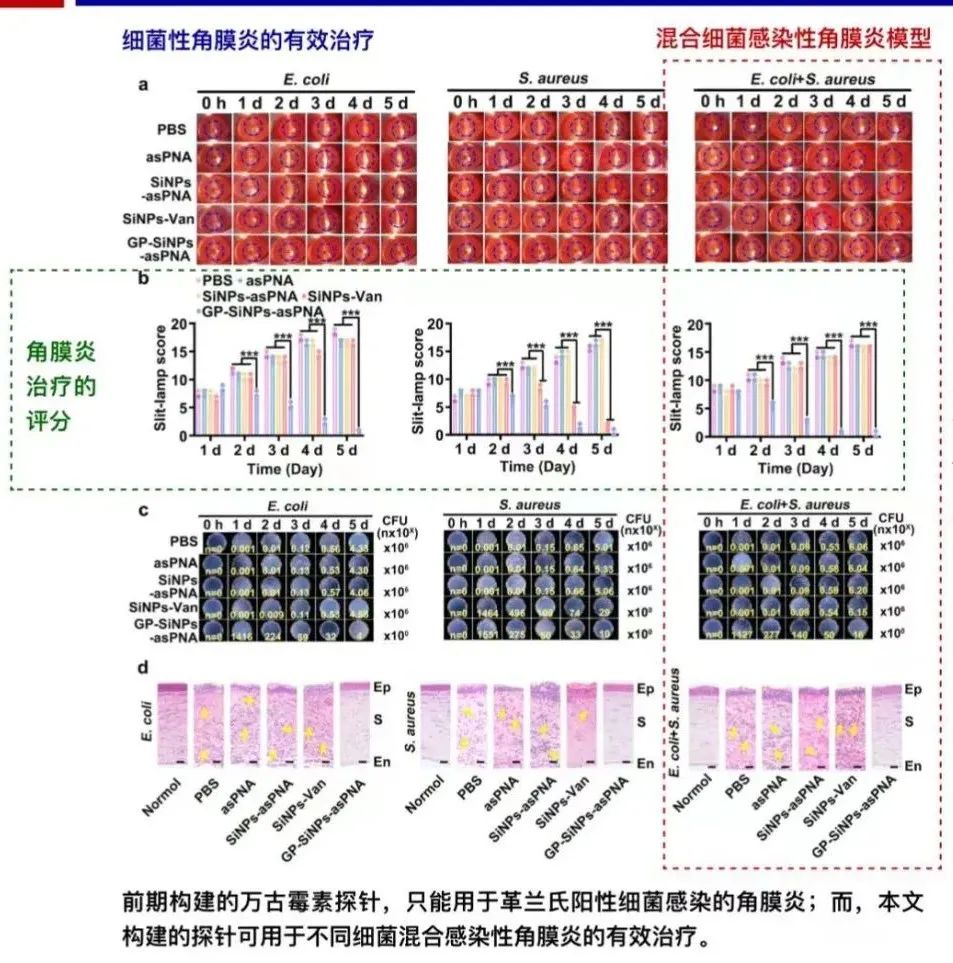
这一策略可以特异性和有效地杀死几乎100%的抗生素耐药(ABR)细菌。此外,该治疗策略对细菌性角膜炎和眼内炎也有明显疗效。这一策略成功地将ASO技术扩大到了哺乳动物细胞以外的细菌中。
在古希腊神话中,希腊联军围困特洛伊城,却久攻不下,于是假装撤退,并留下一具巨大的木马,特洛伊守军把木马运进城中作为战利品。木马中躲藏的希腊士兵打开城门,导致特洛伊沦陷。后人常用“特洛伊木马”(Trojan Horse)来比喻在敌方埋下伏兵里应外合的活动。
早在1980年代,科学们家们提出了抗生素的“特洛伊木马”策略,将抗生素与铁载体结合,从而通过细菌的铁转运系统将抗生素转运到细菌细胞内。但目前还没有研究利用“特洛伊木马”策略将ASO选择性转运到细菌细胞中。
自从发现细菌特异性ATP结合盒(ABC)糖转运蛋白的30年以来,科学家们已经阐明了碳水化合物进入细菌细胞的选择性内化机制。基于这种摄取机制,研究团队已经证明了葡萄糖聚合物(GP)修饰的纳米探针可以通过细菌特异性ABC糖转运蛋白途径内化到各种细菌中。但目前还没有将其应用于向细菌细胞中递送ASO。
在这项最新研究中,研究团队将细菌特异性ABC糖转运蛋白应用于向细菌递送ASO,包括人类来源的抗生素耐药(ABR)细菌,例如多重耐药大肠杆菌(MDR E. coli)、耐甲氧西林金黄色葡萄球菌(MRSA)。
通常情况下,葡萄糖聚合物(GP)和反义多肽核酸(asPNA)修饰的硅纳米颗粒(GP-SiNPs-asPNA)通过细菌特异性ABC糖转运体途径被多种细菌选择性、高效强吞噬。而ABC糖转运体突变的细菌则很难内化GP-SiNPs-asPNA。
在反义多肽核酸(asPNA)进入细菌后,通过与靶点互补配对,选择性抑制细菌基因的表达。结果显示,100%的人类来源的抗生素耐药(ABR)细菌被选择性和有效地杀死。此外,该治疗策略对细菌性角膜炎和眼内炎也有明显疗效。这一策略成功地将ASO技术扩大到了哺乳动物细胞以外的细菌中。
围绕角膜病生物治疗的关键临床问题,复旦大学附属眼耳鼻喉科医院洪佳旭主任在之前病毒性角膜炎的CRISPR基因编辑疗法走到临床IND的基础上,在眼科耐药菌的创新ASO基因治疗研究中再获突破。洪佳旭主任从临床发现问题,再到实验室研究中与苏州大学何耀教授团队合作通过创新材料解决耐药菌问题,二者建立了闭环的科研协作模式,也将在未来积极探索真实世界临床应用可能。

本文地址://www.styjt.com/jiankang/2023-04-26/639505.html
友情提示:文章内容为作者个人观点,不代表本站立场且不构成任何建议,本站拥有对此声明的最终解释权。如果读者发现稿件侵权、失实、错误等问题,可联系我们处理
- 首款渐冻症反义核苷酸疗法获批上市2023-04-26 18:00:34
- Nature:揭示黏连蛋白、CTCF和DNA张力在染色体空间组装中的作用2023-04-26 18:00:33
- Nature:开发出新方法观察癌症相关基因突变中染色质相互作用的变化2023-04-26 18:00:33
- Nature:揭示靶向TCL1A有望阻止血癌产生2023-04-26 18:00:32
- Nature:揭示Smc5/6复合物驱动DNA环挤压机制2023-04-26 18:00:31

 70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗
70岁以上老人核酸检测费用多少 新规定明天起不做核酸了吗2022-11-07

 梅婷现任70岁老公曾剑个人资料(曾剑个人资料)
梅婷现任70岁老公曾剑个人资料(曾剑个人资料)2022-09-08
- 烟台今天已封闭的小区 烟台现在封闭小区名单有哪些
2022-10-12 09:07:30
- 张家界桑植新娘吴梅婚纱照事件完整版 看女主出轨聊天内容视频
2022-11-11 14:27:00
- 无人售货机功能(无人自动售货机操作方法介绍)
2022-07-27 08:41:09
- 目前南岸区及江北封闭小区名单有哪些 看最新封控通告
2022-11-11 14:49:26
- 2022南宁封控小区名单表 南宁最新封闭小区名单2022年8月什么情况
2022-08-26 09:52:30
文章排行榜
- 周排名
- 月排名
- 1北京大学人民医院神经内科罕见病系列报导之三—— 北京大学人民医院首例患者接受伊奈利珠单抗治疗视神经脊髓炎(NMOSD)
- 22023,贝参药业携手善医美多维赋能第三终端攻克咳喘
- 3“新冠二阳”冲上热搜!张文宏呼吁“做好药物储备”
- 4网传高校女学生被3名黑人性侵 校方辟谣称已报警处理
- 5当天种牙当天用! 5月8日,德中口腔这场盛会别错过
- 6竞逐“颠覆性技术”,桐树基因斩获 2022 年全国颠覆性技术创新大赛总决赛优秀奖
- 7世界读书日关心孩童学业 云南白药益生菌儿童牙膏关爱孩童口腔健康
- 82023年欧洲睡眠与呼吸大会召开,韩博学医生应邀参加
- 9神经酰胺CERT评分预测心血管风险引发讨论 背后研发公司Zora浮出水面
- 10从“本质研究”出发创造优质产品 花王(中国)参展2023年中国中西医结合学会 分享研发成果